Es el Primer biológico aprobado en Estados Unidos y la Unión Europa con más de 15 años de experiencia clínica.2
Está indicado como tratamiento en adultos y niños ≥6 años con asma alérgica moderada a grave, siendo elegibles cuando:1,3,4
- Tiene síntomas persistentes a pesar de dosis elevadas de corticosteroides
- Tiene sensibilidad a alérgenos inhalados, diagnosticada en pruebas cutáneas o específicas a IgE.
- Tiene niveles de IgE en sangre dentro del rango de dosis.
- Ha tenido más de un número específico de exacerbaciones en el último año.
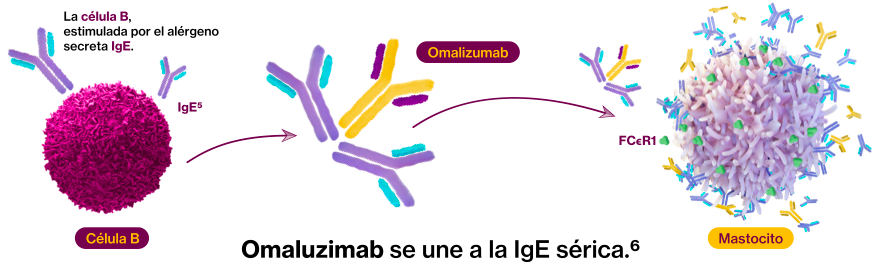
Omalizumab es un anticuerpo monoclonal diseñado para unirse e inactivar la IgE.3
Si requiere de una terapia 4-5 en el escalón GINA.5
Uso de corticoesteroide sistémico por >50% del año previo.5
No se logra control con tratamiento adecuado a dosis máximas.5
- Mal control de síntomas ACQ >1.5, ACT <20.
- Exacerbaciones severas frecuentes con 2 o más rondas de corticoesteroides sistémicos en el último año.
- Exacerbaciones serias que requieren hospitalización, UCI o ventilación mecánica en el último año.
- Limitación del flujo aéreo con FEV1 <80% después de broncodilatador.
ACQ: Cuestionario del control del asma; ACT: Prueba de control de asma; UCI: Unidad de cuidados intensivos; FEV1: Volumen respiratorio forzado en 1 segundo.
Exacerbaciones frecuentes
Mayor alteración de la función pulmonar
Mala calidad de vida
Alto riesgo de efectos secundarios
Más visitas a urgencias y hospitalizaciones
Mayor ausencia escolar y laboral
Material exclusivo para el profesional de la salud.
Las imágenes no corresponden a pacientes o profesionales de la salud reales.
No. de Reg. 251M2006 SSA IV Content ID: FA-11355768 Fecha de vigencia: 23/10/26 No. de Aviso: 2509052002C00136